Fe2O3和Fe3O4有哪些详细区别及形成方式?
Fe2O3与Fe3O4,作为铁的两种氧化物,在日常生活和工业生产中扮演着重要角色。虽然它们都由铁和氧元素组成,但在性质、形态和用途等方面存在着显著的差异。下面,我们将从它们的详细区别和形成方式两个方面,以通俗易懂的方式展开介绍。

Fe2O3与Fe3O4的详细区别
1. 颜色与形态
Fe2O3,通常被称为三氧化二铁或氧化铁,是一种红棕色的粉末。它是铁锈的主要成分,常常可以在铁制品生锈后看到其痕迹。相比之下,Fe3O4,即四氧化三铁,别名磁性氧化铁、氧化铁黑,是一种具有磁性的黑色晶体。这使得两者在外观上能够轻松区分。
2. 化学性质
在化学性质上,Fe2O3与Fe3O4也有显著的不同。Fe2O3具有两性,既能与酸反应生成Fe(Ⅲ)盐,也在强碱介质中表现出一定的还原性,可被强氧化剂氧化。而Fe3O4在潮湿的空气中容易氧化成Fe2O3,但在高温下,它可以与还原剂如氢气(H2)、一氧化碳(CO)、铝(Al)等反应。
3. 化合价与结构
从化合价的角度来看,Fe2O3中铁的化合价为+3价,而Fe3O4中铁的化合价较为复杂,它既有+2价也有+3价。这种化合价的不同也导致了它们在晶体结构上的差异。
4. 用途
由于Fe2O3与Fe3O4在性质上的不同,它们在工业生产和日常生活中的应用也有所不同。Fe2O3常用作颜料、抛光剂、催化剂和红粉等。其鲜艳的红色使其成为重要的颜料成分。而Fe3O4则因其磁性而广泛应用于制造录音、录像磁带和电讯器材等领域,同时也是重要的磁性材料。
Fe2O3与Fe3O4的形成方式
Fe2O3与Fe3O4的形成过程涉及到多种化学反应和条件,以下是一些主要的形成方式。
1. Fe2O3的形成
铁与氧气的反应:在常温下,铁与氧气反应的主要产物是Fe2O3。这是铁生锈的基本原理,也是Fe2O3在自然环境中广泛存在的原因。化学反应方程式为:4Fe + 3O2 = 2Fe2O3。
氢氧化铁的分解:氢氧化铁(Fe(OH)3)在加热或自然干燥的过程中会失去水分,形成Fe2O3。化学反应方程式为:2Fe(OH)3 = Fe2O3 + 3H2O。
其他化学反应:Fe2O3还可以通过其他化学反应生成,如氯化亚铁(FeCl2)与氧气反应、硫化亚铁(FeS2)与氧气反应等。这些反应在工业生产中有一定的应用。
2. Fe3O4的形成
高温下铁与氧气的反应:在高温条件下,铁与氧气直接反应可以生成Fe3O4。这是炼铁过程中常见的一种反应。例如,在高炉炼铁时,铁矿石中的铁与焦炭和空气中的氧气反应,生成铁和Fe3O4。
铁的氧化:在潮湿环境中,铁与氧气接触会发生氧化反应,形成铁锈。虽然铁锈的主要成分是Fe2O3·H2O(即水合三氧化二铁),但在某些特定条件下,Fe2O3可以进一步氧化生成Fe3O4。
火灾中的生成:在火灾高温条件下,铁或钢结构的材料会与氧气反应,生成Fe3O4。这种反应通常会导致建筑结构强度的降低,是火灾对建筑物破坏的重要原因之一。
电化学腐蚀:在电化学腐蚀过程中,铁作为阳极失去电子形成铁离子,而氧气作为阴极接受电子形成氢氧根离子。铁离子与氢氧根离子结合可以生成Fe3O4。这是铁制品在潮湿环境中发生腐蚀的一种机制。
实验室合成:在实验室中,可以通过化学气相沉积(CVD)、溶胶-凝胶法、高温固相反应等方法控制反应条件,合成Fe3O4纳米材料。这些材料在磁性存储、催化剂、锂电池电极等领域有广泛应用。
Fe2O3与Fe3O4的制备与应用实例
为了更好地理解Fe2O3与Fe3O4的制备和应用,我们可以看一些具体的实例。
1. Fe2O3的制备与应用
制备:Fe2O3的制备通常采用湿法或干法。湿法制品结晶细小、颗粒柔软、较易研磨,易于作颜料;干法制品结晶大、
- 上一篇: 部队火锅的美味家常制作方法
- 下一篇: 掌握高效秘诀,轻松变身作业狂人!
-
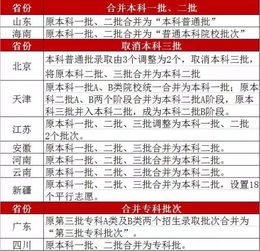 一本和二本大学究竟有哪些区别?新闻资讯10-27
一本和二本大学究竟有哪些区别?新闻资讯10-27 -
 详解音节与音序的区别及音序定义新闻资讯10-21
详解音节与音序的区别及音序定义新闻资讯10-21 -
 民谣吉他和古典吉他有哪些区别?新闻资讯12-21
民谣吉他和古典吉他有哪些区别?新闻资讯12-21 -
 PNG格式图片与JPG格式图片有哪些区别?新闻资讯10-31
PNG格式图片与JPG格式图片有哪些区别?新闻资讯10-31 -
 硬卧和软卧之间到底有哪些主要区别?新闻资讯10-29
硬卧和软卧之间到底有哪些主要区别?新闻资讯10-29 -
 揭秘麻将高手必知技巧:明杠与暗杠的区别到底是什么?新闻资讯11-14
揭秘麻将高手必知技巧:明杠与暗杠的区别到底是什么?新闻资讯11-14